w88优德陈妍/张勇团队首次通过系统评价编码狂犬病毒糖蛋白G(RABV-G)mRNA疫苗的免疫原性及保护率,揭示RABV-G不同结构域对mRNA疫苗免疫效率的影响,随后进一步优化mRNA疫苗与灭活病毒疫苗的异源免疫策略并探究相关机制,为增强狂犬疫苗的快速应答和持续保护提供新思路。研究成果于2025年3月1日在疫苗学期刊《Npj Vaccines》在线发表,题为“Optimizing rabies mRNA vaccine efficacy via RABV-G structural domain screening and heterologous prime-boost immunization”。

狂犬病是由狂犬病毒(RABV)引起的致死性人畜共患病,其致死率接近100%。目前使用的灭活疫苗(IRV)虽有效,但存在生产成本高、需多次接种等问题。mRNA技术在疫苗领域的应用为狂犬病毒的预防提供了新的方向。RABV-G是中和抗体的主要靶点,但其结构域(胞质域、跨膜域、胞外域)对mRNA疫苗免疫原性的影响尚不明确。该研究制备了编码全长RABV-G(RABV-Full)、RABV-R333Q、胞外域/跨膜域(RABV-TE)和胞外域(RABV-E)的狂犬mRNA疫苗。对mRNA疫苗诱导小鼠的免疫应答和保护率进行评价,结果显示RABV-Full和RABV-R333Q诱导了高效的体液和细胞免疫,并提供完全保护,RABV-TE的中和抗体和保护率(70%)则明显降低,而RABV-E则几乎不产生中和抗体。研究发现,mRNA疫苗虽然在第二次免疫后可诱导比IRV更高的中和抗体,但IRV初次免疫后诱导的短期抗体水平却明显高于mRNA疫苗。据此,该研究设计利用异源免疫策略将两种疫苗平台的优势结合,以期提升疫苗的短期和长期免疫应答水平。研究结果显示,IRV初免-RABV-Full加强(IRV>RABV-Full)组的早期中和抗体快速升高,长期效价稳定,攻毒保护率100%;而RABV-Full初免-IRV加强(RABV-Full>IRV)组的长期中和抗体水平更高,但早期应答较弱,攻毒保护率为90%。转录组分析表明,mRNA疫苗可同时激活MHC I和MHC II抗原呈递通路及B/T细胞活化,而IRV主要激活MHC II通路,驱动B细胞分泌抗体,T细胞反应较弱。综上,该研究证实,编码全长RABV-G的mRNA疫苗(无论是否含R333Q突变)均可诱导较强的体液/细胞免疫并实现完全保护,RABV-G的胞质域虽非中和抗体产生的必需结构,但对提升疫苗免疫原性和保护效率至关重要;异源免疫策略IRV>RABV-Full可整合IRV早期高效中和抗体优势与mRNA疫苗长效免疫特性。该研究为狂犬mRNA疫苗的序列设计和免疫策略优化提供了重要依据。
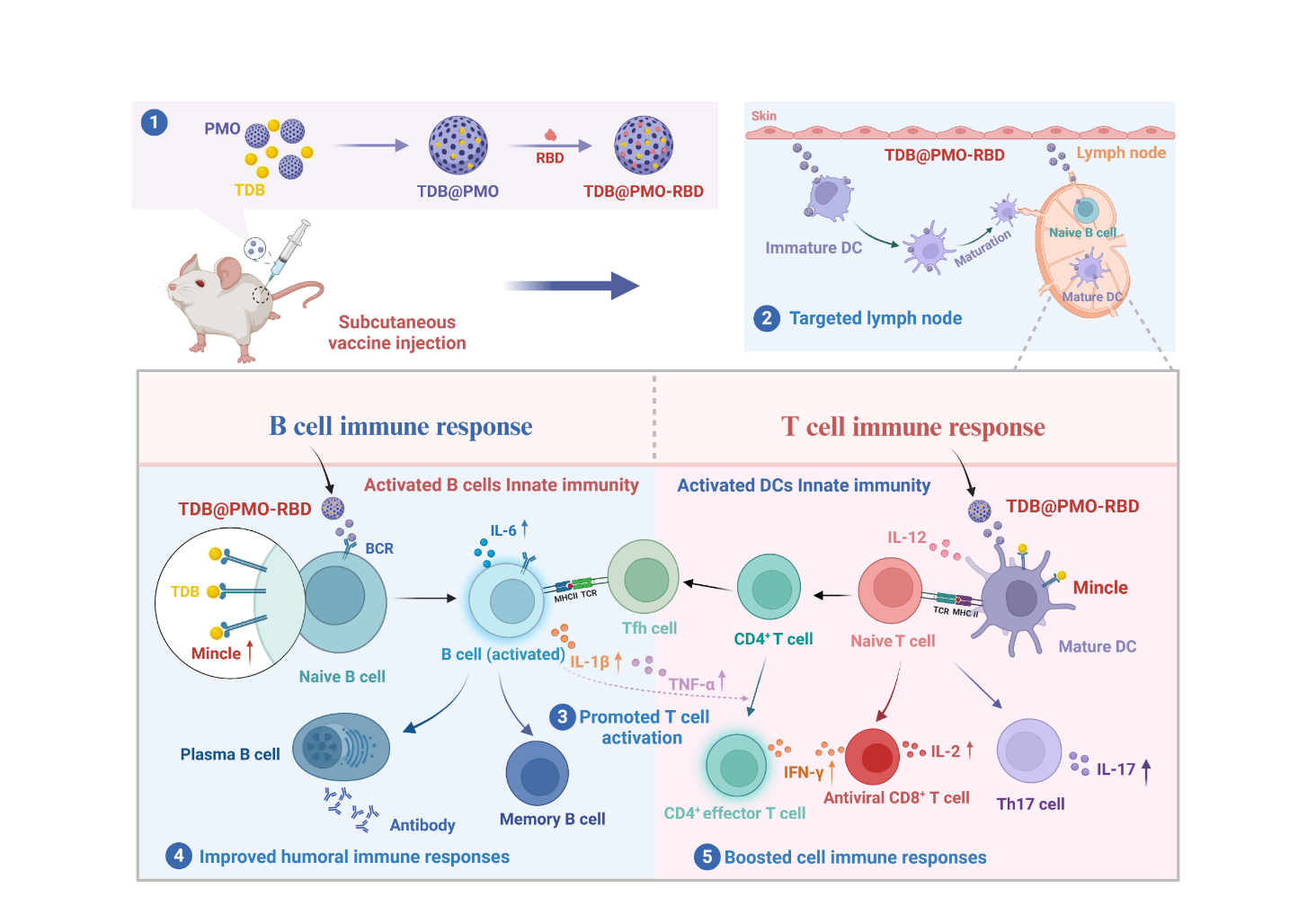
图:狂犬mRNA疫苗与灭活疫苗异源免疫策略(左)及免疫微环境分析
论文第一完成单位为w88优德,第一作者为w88优德博士生李冬冬,w88优德陈妍教授和张勇副教授为该论文的共同通讯作者。
原文链接:https://www.nature.com/articles/s41541-025-01098-w